上海科学家构建双重功能“骨类器官”,为股骨头坏死等疾病治疗带来希望
来源:上观新闻 作者:解放日报 俞陶然
上海在硬组织类器官领域已形成自主技术体系。
你听说过“类器官”吗?最近,上海大学、上海交通大学医学院附属新华医院苏佳灿教授团队的两项科研成果发表在材料科学国际权威期刊《先进材料》和《生物活性材料》上,解析了骨类器官生命全周期发育规律,并成功构建了兼具血管化与矿化功能的骨类器官,为骨再生医学和疾病模型研究提供了系统性解决方案。未来3—5年,上海科研团队计划将这些实验室成果应用于临床,治疗骨缺损、股骨头坏死等骨科疑难疾病。
所谓类器官,是利用成体干细胞或多能干细胞进行体外三维培养,所形成的具备一定空间结构的组织类似物。类器官的“类”字意味着它并不是真的人体器官,但可以在结构与功能上模拟真实的器官,并能进行长期稳定的传代培养。过去十余年,多种类器官已在实验室里诞生。2018年,《自然·方法》杂志将类器官技术评为“年度方法”。
能否利用这种技术培育出骨类器官?2022年,苏佳灿教授团队在国家自然科学基金重点项目的支持下,结合3D打印技术开发出骨类器官1.0版,验证了其在骨缺损修复中的潜力。
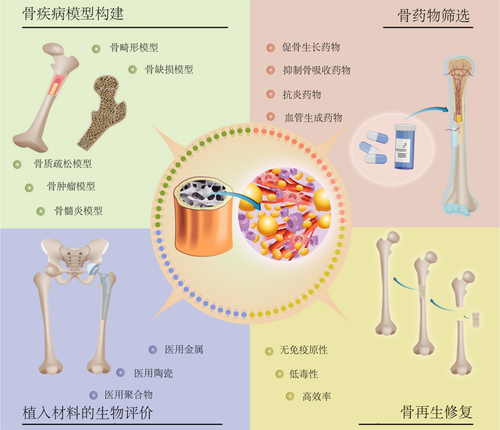
骨类器官在骨疾病中的应用
在此基础上,科研团队提出“材料生物学效应”驱动策略,开始研发普适性仿骨基质,希望这种构造骨类器官的基础材料像输液液体一样,今后能适用于众多骨缺损、股骨头坏死等患者。经过长期探索,他们成功引导干细胞自主分化为成骨谱系细胞,并自发形成矿化胶原基质共嵌结构,再现了胚胎骨骼发育模式。
基于这种仿骨基质构建的骨类器官,在体外展现出完整的生命周期演化,而且在小鼠模型中表现出卓越的骨整合能力,为骨再生研究提供了标准化模板。“这种仿骨基质能实现‘材料生物学效应’,可以与人体组织细胞融合、发生反应。”苏佳灿说。
在攻克结构仿生难题后,他们开始研究类器官的功能化难题,希望骨类器官的功能与真实的骨头基本一致。“如果把骨骼比作摩天大楼,血管就是贯穿其中的物流网络。”苏佳灿说,当骨类器官的尺寸超过400微米时,血管网络对氧气、营养和信号分子传输至关重要。然而,在生物学领域广泛使用的Matrigel基质存在免疫原性高、力学性能不足等问题,难以支撑骨类器官的血管化构建。
矿化骨类器官、血管化骨类器官研究示意图
针对这个问题,上海科研团队通过提取骨源脱细胞外基质(ECM),结合光交联与动态自组装技术,开发出工程化ECM-DNA-CPO仿骨基质凝胶;再利用“体外动态培养+体内异位骨化”双模式策略,最终实现了矿化骨与血管系统的同步发育。这意味着,骨类器官在生长、矿化过程中,血管网络会在其中发育,为骨细胞提供氧气、营养和各种信号分子。
这一突破使骨类器官从结构仿生迈向功能重建,为骨坏死、类风湿性关节炎等复杂骨病的机制研究与治疗奠定了基础。今后,科研人员可利用这种骨类器官开发疾病模型,并进行药物筛选,开发治疗复杂骨病的创新药物。
中国科学院院士、上海大学校长刘昌胜表示,上海大学以生物医药前沿为战略核心,通过搭建医工交叉研究院打破研究壁垒,布局“智能诊断—精准治疗—智慧康复”创新链,已构建覆盖基础研究到产业转化的科研矩阵。依托转化医学院类器官研究中心和转化医学国家科学中心(上海)平台,苏佳灿团队将推动骨类器官沿生理型、病理型、结构型、复合型和应用型方向阶梯式发展。近日发表的两项研究成果,标志着上海在硬组织类器官领域已形成自主技术体系。未来,科研团队将聚焦“血管—神经—免疫多维调控”机制,推动骨类器官在个性化医疗、药物筛选等场景的应用落地,为再生医学带来范式变革。