开年顶刊!交大团队Cell发文,首次揭示这一重要分子机制
来源:上海交通大学
北京时间2026年1月3日
上海交通大学Bio-X研究院曹骎研究团队
与上海交通大学医学院附属新华医院张飞团队合作
在《细胞》(CELL)上在线发表了题为
“Structure of pancreatic hIAPP fibrils derived from patients with type 2 diabetes”的研究论文
研究团队首次报道了来源于2型糖尿病患者胰腺组织中的hIAPP纤维的冷冻电镜结构
为理解2型糖尿病的病理机制及开发靶向治疗策略提供了关键结构依据
2型糖尿病(type 2 Diabetes,T2D)是一种全球高发的代谢性疾病,影响着全球近10%人口的健康与寿命。其发病机制复杂,涉及胰岛素抵抗和胰岛β细胞功能进行性衰竭。在β细胞衰亡过程中,所分泌的人胰岛淀粉样多肽(human islet amyloid polypeptide, hIAPP)会发生错误折叠与异常聚集,在胰岛内形成淀粉样沉积。这一病理现象在超过90%的2型糖尿病患者胰腺中被观察到,被广泛认为与β细胞毒性、胰岛素分泌功能障碍及疾病进展密切相关。因此,如可延缓hIAPP纤维化或清除已形成的hIAPP纤维,将有可能对于2型糖尿病的治疗提供帮助。尽管以往研究已获得体外制备的hIAPP纤维结构,但由于淀粉样纤维组装的特殊性,相同蛋白在不同条件下往往会形成不同结构的纤维。因此病人体内形成的hIAPP纤维是否与体外hIAPP纤维具有一致的分子结构尚不清楚。hIAPP病理性结构的缺失极大地制约了以hIAPP为靶点的糖尿病药物开发。
另辟蹊径,破解样品获取难题
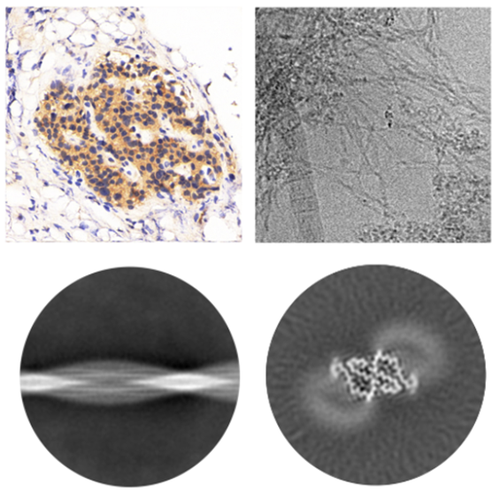
hIAPP病理性结构缺失的主要原因之一是病人胰腺样品获取困难,因为糖尿病治疗并不需要涉及胰腺相关手术或穿刺活检等。为解决这一难题,研究团队提出一种另辟蹊径的解决方案,即在因为其它疾病(如胰腺癌等)需要手术切除部分胰腺的患者中寻找同时患有2型糖尿病的患者,并在获取患者知情同意的情况下使用切除胰腺组织的癌旁正常组织作为研究样本。基于这一方案,研究团队共收集到了六位捐献者的胰腺组织,并针对胰腺组织中淀粉样纤维含量低、提取困难的技术挑战,优化了一套温和而高效的提取纯化流程,对六位捐赠者的组织分别进行了纤维提取。研究团队发现,仅在四位患有2型糖尿病的捐献者的胰腺组织提取物中观察到了具有淀粉样纤维形貌的纤维(图1),在两位未患糖尿病的捐献者胰腺组织提取物中则未观察到类似纤维,提示了此纤维与糖尿病的紧密关联。
图1 病人胰腺中hIAPP纤维的提取及结构解析。左上:病人胰腺切片的hIAPP免疫组化分析;右上:胰腺提取物的冷冻电镜图片;下:纤维冷冻电镜数据的二维分类及三维重构。
首次揭示患者体内病理性蛋白纤维结构
为糖尿病诊疗药物开发提供重要结构基础
成功提取得到病理性纤维后,研究团队利用冷冻电镜技术对提取的纤维进行了结构解析,并成功得到其中三位捐献者的纤维结构(分辨率分别为2.9 Å、3.0 Å及3.4 Å)。
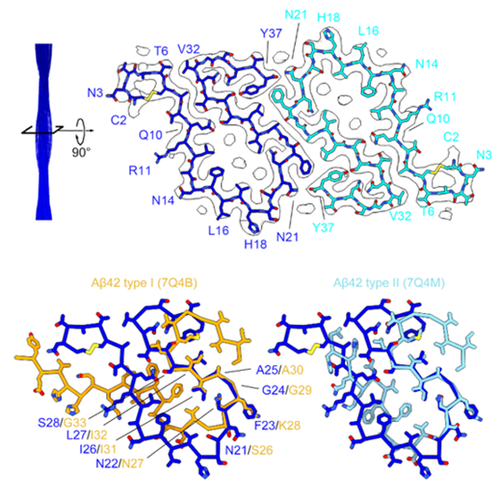
结构分析表明,来自三位捐献者的纤维具有几乎相同的结构。它们由两股对称的原纤维丝缠绕而成。其核心区域包含hIAPP的第2-37位残基,并形成了一种此前未被报道的独特“Ω形”折叠模式(图2)。与此前报道的体外hIAPP纤维相比,该结构在主链走向、侧链组装及分子内相互作用网络方面均存在显著差异,凸显了体内病理环境的独特性及其对蛋白质错误折叠途径的特异性影响。在解析出的结构中,研究团队清晰辨识出多处非蛋白源性密度,它们对称地分布于纤维表面特定的口袋或其内部空腔中,提示了内源性小分子配体的结合。其中分布于内部空腔的密度被hIAPP的疏水性侧链所环绕,提示在此处结合的配体可能是脂类物质或其它疏水分子。这些配体可能在体内起到稳定纤维构象、调节纤维生长动力学或介导细胞毒性等作用,为理解hIAPP的病理活性提供了全新的结构视角。同时,分布于纤维表面的密度提示了一些潜在的配体结合口袋,可作为设计小分子抑制剂、抗体类药物或干扰肽的特异性靶点,旨在阻止病理性纤维的形成或促进其解聚,从而对于糖尿病的治疗提供帮助。
图2 hIAPP纤维结构(上)及其与AD病人脑中Aβ纤维结构比较(下)
发现与阿尔茨海默病的分子关联
为跨疾病共诊共治提供理论依据
此外,2型糖尿病与阿尔茨海默病(Alzheimer’s disease,AD)之间的临床关联已有记载,即2型糖尿病患者往往有更高机率患上阿尔茨海默病,反之亦然。有假说认为这一临床关联源自于hIAPP纤维和阿尔茨海默病中的Aβ纤维之间存在体内交叉播种效应。即2型糖尿病患者胰腺内的hIAPP纤维可能会通过胰腺与大脑间的神经连接促进其脑内Aβ的纤维化,从而引发阿尔茨海默病,反之亦然。研究团队通过结构比较发现,hIAPP纤维的核心折叠单元与阿尔茨海默病病人脑中Aβ纤维具有显著的构象相似性,两种纤维在一个8残基片段中显示出几乎相同的构象(图2),这个片段可能作为hIAPP和Aβ之间交叉播种的保守模板。这一发现为hIAPP与Aβ的体内交叉播种假说提供了结构解释,同时为两种疾病的“共病、共诊、共治”提供了理论依据。
本研究成功建立了一套从复杂人体组织中提取、纯化并解析低丰度病理蛋白纤维的技术流程,首次在原子水平上揭示2型糖尿病患者体内hIAPP淀粉样纤维的高分辨率结构。该结构为针对2型糖尿病中hIAPP淀粉样变的治疗策略开发奠定了坚实基础。研究获得了科技部重点研发计划、国家自然科学基金、上海交通大学医工交叉项目、“永新青年学者”等项目资助。